Повторные неудачи в ЭКО. Часть IV
Что делать при повторных неудачах?
- Предимплантационный генетический скрининг (ПГС)
- Количество эмбрионов на перенос
- Тест оценки рецептивности эндометрия (ERA)
- Гистероскопия
- Локальная травма эндометрия
- Мононуклеары периферической крови+ХГЧ и другие.
Причин повторных неудач много, возможно это не одна причина, а сочетание нескольких. С другой стороны мы в своих ресурсах ограничены. У нас нет бесконечного количества терпения, здоровья, денег и, самое главное, времени. Поэтому выбирать нужно самые вероятные, наиболее короткие пути решения. Потратив время на что – то малозначимое, мы можем упустить время для чего –то важного. Главным в тактике является выбор приоритетов, тех самых наиболее коротких путей. Начинать следует с наиболее вероятной причины в каждой конкретной ситуации.
И без статистики нам не обойтись.
Ниже представлена таблица зависимости вероятности наступления беременности от количества эмбрионов и возраста. Цифры я брал из собственных данных. Разделил количество увиденных плодных яиц на количество перенесенных эмбрионов и разгруппировал по возрастным группам. Зная вероятность прикрепления одного эмбриона, примерно посчитал вероятность наступления беременности при определенном количестве эмбрионов, не обязательно перенесенных за один раз(!).
Вероятность наступления беременности на одну пункцию в зависимости от возраста и количества полученных бластоцист.
| Количество эмбрионов | Возраст | ||
| до 35 | 36-39 | 40 -42 | |
| 1 | 45% | 22% | 11% |
| 2 | 70% | 39% | 21% |
| 3 | 83% | 53% | 30% |
| 4 | 91% | 63% | 37% |
| 5 | 95% | 71% | 44% |
| 6 | 97% | 77% | 50% |
| 7 | 98% | 82% | 56% |
| 8 | 99% | 86% | 61% |
| 9 | 100% | 89% | 65% |
| 10 | 100% | 92% | 69% |
Как Вы видите есть существенная разница между различными возрастными группами. И эта разница будет влиять на тактику.
С чем же связана такая разница?
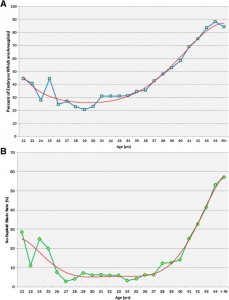
В 2014 году была опубликована статья, касающаяся изучения кариотипа (набора хромосом) эмбрионов . Было проанализировано более 15 тыс. эмбрионов. И получили следующие данные. Они на нижних двух графиках. На первом изображена кривая отражающая долю анэуплодиных (имеющих неправильный набор хромосом) эмбрионов в зависимости от возраста женщины. Имеется четкий тренд к увеличению количества аномальных эмбрионов в возрасте старше 35 лет. Если в возрасте 31-34 лишь треть эмбрионов имеет анэуплоидию, то в возрасте 44 лет достигает почти 90%, т.е. лишь один из десяти эмбрионов будет иметь нормальный кариотип. В группе 35-40 происходит постепенное двукратное увеличение вероятности получения анэуплодиных эмбрионов , т.е. чем ближе к 40 годам, тем ниже вероятность получения нормального эмбриона.
Второй график не менее интересен, а с учетом нашей темы даже более важен. Здесь показана вероятность отсутствия эуплодиных (с нормальным кариотипом) эмбрионов в зависимости от возраста. В любом возрасте есть определённая пропорция пациентов, у которых может не быть ни одного эуплодиного эмбриона. Даже в молодом возрасте, до 35 лет, где обычно два из трех эмбрионов имеют нормальный набор хромосом, у каждой двадцатой пациентки может не быть ни одного эмбриона с нормальным кариотипом. Правда это не значит, что в следующей программе ЭКО тоже не будет ни одного эмбриона с нормальным кариотипом.
Как уровнять шансы эмбрионов от матерей разного возраста?
 Единственный способ уровнять шансы эмбрионов и действительно говорить о нормальных эмбрионах хорошего качества — это провести предимплантационный генетический скрининг (ПГС), часто путают с термином ПГД – предимплантационная генетическая диагностика. Т.е. если мы будем знать о кариотипе эмбриона мы не перенесем эмбрион заведомо обреченный на неудачу.
Единственный способ уровнять шансы эмбрионов и действительно говорить о нормальных эмбрионах хорошего качества — это провести предимплантационный генетический скрининг (ПГС), часто путают с термином ПГД – предимплантационная генетическая диагностика. Т.е. если мы будем знать о кариотипе эмбриона мы не перенесем эмбрион заведомо обреченный на неудачу.
С целью выяснения кариотипа следует использовать наиболее информативные и безопасные для эмбриона методики. А именно – биопсия трофоэктодермы и анализ на все хромосомы с помощью сравнительной геномной гибридизации (aCGH) или секвенирования следующего поколения (NGS).
В какой ситуации проводить ПГС?
Ответ зависит в первую от возраста женщины.
До 35 лет мы понимаем, что скорее всего две из трех бластоцист будут иметь нормальный кариотип и как следствие высокие шансы на имплантацию. Так при переносе 4 эмбрионов мы имеем шанс порядка 90% (за два, три или четыре переноса). Если беременность не наступит, я буду думать о других причинах и искать в них ответ (об этом ниже). При отсутствии беременности после переноса 6-8 бластоцист я буду думать о проведении ПГС. У нас ведь есть группа женщин молодого возраста, у которой может не быть ни одного эмбриона для переноса. В моей практике нет ни одной пары, у которой не наступили беременности, если мы за одни раз получили 8 и более бластоцист.
У женщины старше 40 лет значимо снижаются шансы на то, что эмбрионы имеют нормальный набор хромосом. Рассматривая проблему повторных неудач в ЭКО, я сразу буду рекомендовать проведение ПГС женщине в возрасте старше 40 лет. Это существенно ускорит наш путь к достижению цели.
При повторных неудачах в возрасте 35-40 тактика будет зависеть от того к какой возрастной границе женщина ближе.
В конечном итоге выбор будет зависеть от конкретной ситуации.
Итак, к каким выводам меня приводят эти размышления:
- Возраст матери до 35 лет — ПГС при отсутствии беременности после переноса 6-8 бластоцист.
- 35-40 лет ПГС обсуждать сразу, применять после неудачного переноса 8 эмбрионов или раньше в зависимости от ситуации.
- Старше 40 лет сразу ЭКО с проведением ПГС.
Сколько эмбрионов переносить?
 Очевидно, что чем больше мы перенесем эмбрионов в полость матки, тем больше шансы на наступление беременности. Такой поход был распространен еще совсем недавно. Связано это было с недостаточно эффективной криоконсервацией – эмбрионы погибали в процессе «заморозки» и «разморозки», поэтому и старались перенести все, что было. Главная проблема, связанная с таким подходом – резкое увеличение многоплодия и связанных с ним осложнений беременности. По мере развития технологии ЭКО, в частности криоконсервации, удалось решить проблему многоплодия без потери результативности ЭКО. Сегодня самым правильным подходом сегодня с медицинской точки зрения является перенос одного эмбриона . В связи с этим последние годы огромное внимание уделялось вопросу – какой эмбрион выбрать для переноса? Все это стало назваться селективный перенос одного эмбриона.
Очевидно, что чем больше мы перенесем эмбрионов в полость матки, тем больше шансы на наступление беременности. Такой поход был распространен еще совсем недавно. Связано это было с недостаточно эффективной криоконсервацией – эмбрионы погибали в процессе «заморозки» и «разморозки», поэтому и старались перенести все, что было. Главная проблема, связанная с таким подходом – резкое увеличение многоплодия и связанных с ним осложнений беременности. По мере развития технологии ЭКО, в частности криоконсервации, удалось решить проблему многоплодия без потери результативности ЭКО. Сегодня самым правильным подходом сегодня с медицинской точки зрения является перенос одного эмбриона . В связи с этим последние годы огромное внимание уделялось вопросу – какой эмбрион выбрать для переноса? Все это стало назваться селективный перенос одного эмбриона.
Манипуляции с количеством эмбрионов принципиально ничего не меняют и они не решают проблему повторных неудач в ЭКО.
Что мы можем сделать с эндометрием в случае повторных неудач при ЭКО?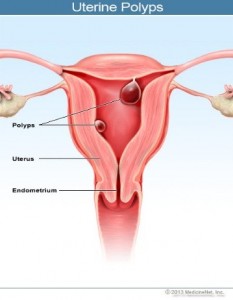
О значимости эндометрии мы будем говорить только тогда, когда перенесли 4 и более эмбриона (бластоцисты хорошего качества, возраст матери до 35 лет либо эмбрионы после ПГС)
По сути есть два направления поиска:
- Обнаружение и коррекция структурных, видимых глазом изменений полости матки.
- Обнаружение и попытка коррекции функциональных нарушений эндометрия (рецептивность).
В первом случае мы можем заглянуть в полость матки, увидеть патологию (полипы эндометрия, синехии (спайки) полости матки, деформации полости матки). Увидеть и исправить эти нарушения можно при гистероскопии. Это именно то обследование, которое следует сделать в случае неудачного ЭКО. Причем нельзя рассматривать УЗИ как альтернативу гистероскопии
Во втором случае есть несколько ответвлений поиска.
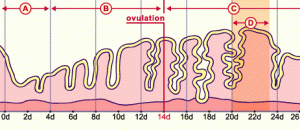
Во-первых, может быть смещено «окно имплантации». Узнать это можно если провести оценку индивидуального окна имплантации. Сделать это можно с помощью тестов, оценивающих время наибольшей «рецептивности» эндометрия, наиболее обещающий тест — Endometrial Receptivity Array Test (ERA).
Во-вторых, «рецептивность» эндометрия может быть увеличена. С этой целью используют «скрэтчинг эндометрия» , введение мононуклеаров периферической крови и ростовых факторов в полость матки перед переносом эмбрионов. Эффективность этих методик, по крайней мере, в руках авторов исследований весьма впечатляющая, они говорят об увеличении эффективности программ в 2-3 раза. Речь идет именно о пациентах, у которых были неудачные повторные переносы эмбрионов (4 и более). Плюсы видны именно в этой маленькой группе
, введение мононуклеаров периферической крови и ростовых факторов в полость матки перед переносом эмбрионов. Эффективность этих методик, по крайней мере, в руках авторов исследований весьма впечатляющая, они говорят об увеличении эффективности программ в 2-3 раза. Речь идет именно о пациентах, у которых были неудачные повторные переносы эмбрионов (4 и более). Плюсы видны именно в этой маленькой группе
 В-третьих, перенос эмбрионов на фоне нормального гормонального фона. Отсутствие «свежего» переноса позволяет выполнить перенос тогда, когда эндометрий готов лучшим образом, а не тогда, когда мы вынуждены выполнить перенос по тем или иным причинам. Выполняя перенос эмбрионов в следующим менструальном цикле, а не в цикле, когда получали яйцеклетки, мы добиваемся нормального уровня гормонального фона, нормального развития эндометрия без избыточно влияния тех или иных гормонов. Однако крайне важным условием является безупречная техника криоконсервации и оттаивания эмбрионов, без этого никаких плюсов добиться не удастся.
В-третьих, перенос эмбрионов на фоне нормального гормонального фона. Отсутствие «свежего» переноса позволяет выполнить перенос тогда, когда эндометрий готов лучшим образом, а не тогда, когда мы вынуждены выполнить перенос по тем или иным причинам. Выполняя перенос эмбрионов в следующим менструальном цикле, а не в цикле, когда получали яйцеклетки, мы добиваемся нормального уровня гормонального фона, нормального развития эндометрия без избыточно влияния тех или иных гормонов. Однако крайне важным условием является безупречная техника криоконсервации и оттаивания эмбрионов, без этого никаких плюсов добиться не удастся.
Заключение.
Идеально выполнение этапов технологии (выбор протокола, стимуляции, пункция, культивирование эмбрионов), перенос в благоприятных условиях эуплодоидных (с нормальным кариотипом) эмбрионов в нормальную полость матки (после гистероскопии и скрэтчинга эндометрия) позволяет помочь 95-98% пациентов с повторными неудачами.
Остальным 2-5% могут понадобится методики с недоказанной эффективностью, или донорство ооцитов или суррогатное материнство, или донорство спермы или чудо.
Читайте также: