-
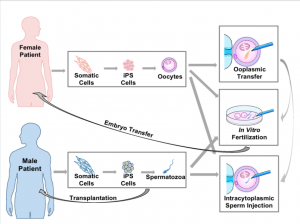
Искусственные гаметы.
 Человек формируется всего из одной оплодотворённой яйцеклетки. Клетка растет, делится, превращается в эмбрион, плод, ребенка и взрослого человека. Но начинается все с одной клетки. Каждая клетка в организме несет в себе информацию обо всех клетках, все клетки имеют одинаковый геном, другими словами набор инструкций везде один и тот же.
Человек формируется всего из одной оплодотворённой яйцеклетки. Клетка растет, делится, превращается в эмбрион, плод, ребенка и взрослого человека. Но начинается все с одной клетки. Каждая клетка в организме несет в себе информацию обо всех клетках, все клетки имеют одинаковый геном, другими словами набор инструкций везде один и тот же.
Почему же мы имеем такое разнообразие клеток, если они вроде как одинаковые. Дело в том, что для каждой клетки активируются определённые гены, и она меняется и внешне и функционально, т.е. каждая клетка начинает выполнять определённый набор инструкций. Клетка двигается по пути специализации, приобретает свойства необходимые для выполнения работы определённого органа, например миоцит – помогает мышце сокращаться, гепатоцит – выделяет необходимые ферменты и создает нужные соединения, остеоцит – формирует кость.
Можно ли повернуть этот процесс вспять? Можно ли направить развитие клетки по нужному нам пути, например, вырастить новую яйцеклетку или сперматозоид?
Оказывается, это возможно. Взяв соматическую клетку (любая клетка в организме, кроме половых) можно ее перепрограммировать и получить яйцеклетку или сперматозоид.
Дальше их использовать для оплодотворения с помощью ЭКО. Т.е. отсутствие половых желез, потеря их функции из-за болезни, возраста, это еще не повод использовать донорские яйцеклетки и сперматозоиды.
В опытах на животных уже получены результаты, т.е. технология работает. Пока мы не знаем обо всех рисках этой технологии. И не можем сказать, когда эта технология может быть использована у людей.
-
Трое родителей – один ребенок.
Для появления нового человека нужны мужчина и женщина. Но иногда для достижения нужного результата нужен третий.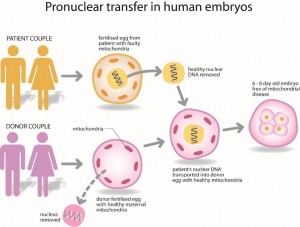
Почти вся генетическая информация находится в ядре клетки, но часть информации хранится в цитоплазме, окружающей ядро. Цитоплазма содержит митохондрии, они несут свою собственную ДНК. Митохондрии достаются человеку всегда от матери. Их функция – энергообеспечение жизнедеятельности клетки. При нарушении этой функции возникают заболевания. Встречаются они редко, но протекают тяжело.
Новая технология позволяет переносить весь генетический материал матери, за исключением дефектного ДНК митохондрий. В результате получается эмбрион, содержащий родительскую информацию в ядре и донорскую информацию в митохондриях.
Как это делается технически?
Спермой мужа оплодотворяют яйцеклетку жены. Одновременно оплодотворяют и яйцеклетку донора яйцеклетки. После оплодотворения яйцеклетки, ядро из донорской яйцеклетки извлекают и помещают туда ядро из яйцеклетки жены. В результате полученный эмбрион имеет родительскую генетику, плюс здоровые митохондрии донора.
В настоящее время технология проходит рассмотрение для проведения клинических испытаний на людях.
Возможно она найдет себе применение не только для лечения митохондриальных заболеваний, но и для решения других проблем. Например, поможет повысить эффективность лечения бесплодия с помощью ЭКО.
-
In vitro activation (IVA): Вторая жизнь яичников?
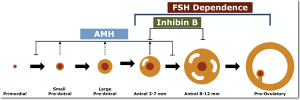
При рождении у девочки есть определённое количество потенциальных яйцеклеток. С годами независимо ни от чего, эти предшественники яйцеклеток исчезают, лишь часть из них дорастает до нормальной яйцеклетки, остальные начав расти, сразу прекращают это делать и атрофируются. Скорость, с которой происходит потеря будущих яйцеклеток, зависит от индивидуальных особенностей. У кого-то быстрее, у кого-то медленнее. При некоторых состояниях потеря происходит очень быстро, развивается синдром раннего истощения яичников. Это состояние, при котором яичники перестают нормально работать уже к 30 годам.
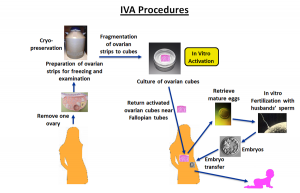 Условно, созревание яйцеклетки можно разделить на две части: первая часть – не зависима от фоликулостимулироующего гормона (ФСГ), вторая — зависит от стимулирующего эффекта ФСГ. До сих пор мы могли воздействовать только на вторую часть, назначая препараты ФСГ. Добраться до фолликулов малого размера, не было возможности. Сегодня разработана технология, позволяющая активизировать и дорастить именно эти мелкие фолликулы. Суть ее в следующем. С помощью операции забирается часть яичника, содержащая эти ранние фолликулы, обрабатывается специальным образом и вводится обратно в яичник. Дальше можно стимулировать с помощью фолликулостимулирующего гормона и получить яйцеклетку и провести ЭКО.
Условно, созревание яйцеклетки можно разделить на две части: первая часть – не зависима от фоликулостимулироующего гормона (ФСГ), вторая — зависит от стимулирующего эффекта ФСГ. До сих пор мы могли воздействовать только на вторую часть, назначая препараты ФСГ. Добраться до фолликулов малого размера, не было возможности. Сегодня разработана технология, позволяющая активизировать и дорастить именно эти мелкие фолликулы. Суть ее в следующем. С помощью операции забирается часть яичника, содержащая эти ранние фолликулы, обрабатывается специальным образом и вводится обратно в яичник. Дальше можно стимулировать с помощью фолликулостимулирующего гормона и получить яйцеклетку и провести ЭКО.
Пионер в этой области доктор Kashiro Kawamura из Японии. Ему удалось дальше всех продвинуться в этой технологии. Благодаря ему на сегодняшний день родилось два ребенка.
-
Искусственная матка.
 Развитие вне полости матки называют эктогенезом. Сама идея возникла почти 100 лет назад. В 1924 году термин эктогенез ввел в обиход британский ученый B.S. Haldane. Он предсказал, что к 2074 лишь треть людей будет рождаться обычным образом.
Развитие вне полости матки называют эктогенезом. Сама идея возникла почти 100 лет назад. В 1924 году термин эктогенез ввел в обиход британский ученый B.S. Haldane. Он предсказал, что к 2074 лишь треть людей будет рождаться обычным образом.
За последние 20-30 лет в этом направлении сделано очень много.
С одной стороны, врачи научились выхаживать детей с 22 недель беременности. Т.е. фактически половину нормального срока развития, ребёнок находится вне матки, т.е. мы уже говорим о частичном эктогенезе. Дальнейшее снижение срока маловероятно. Дело в том что, находясь внутриутробно, ребенок получает кислород, питательные вещества из крови матери. В случае рождения раньше срока ребенку приходится надеется на свои незрелые органы и системы. Используемое оборудование облегчает эту задачу, но не способно решить ее полностью.
С другой стороны, предпринимаются шаги по развитию эмбриона в искусственных условиях. В 2003 году Доктору Хелен Хунг Чинг Лиу удалось довести развитие мышиного эмбриона почти до конца беременности. В 2016 году была опубликована работа о культивировании человеческого эмбриона до 13 суток развития.
Для воплощения идеи искусственной матки необходимо решить множество задач. Наиболее актуальные — создание искусственного эндометрия (место куда прикрепляется эмбрион) и создание искусственных околоплодных вод.
-
Искоренение генетических заболеваний.
 Каждый из нас является носителем 3-4 тяжелых генетических мутаций и нескольких десятков нетяжелых. Если бы мы встретили партнера с такой же мутацией, то мог бы родится ребенок с этим заболеванием, а не просто носительством.
Каждый из нас является носителем 3-4 тяжелых генетических мутаций и нескольких десятков нетяжелых. Если бы мы встретили партнера с такой же мутацией, то мог бы родится ребенок с этим заболеванием, а не просто носительством.
Для того, чтобы «больные» гены проявились нужно их иметь в двух экземплярах, один от матери и один от отца. В противном случае будет носительство «больного» гена, а «здоровый» ген выполнить всю работу и не даст развиться заболеванию.
Самое частое генетическое заболевание – муковисцидоз. Носителем этого заболевания является 1 их 50 человек. Если встречаются два человека носителя заболевания, вероятность рождения больного ребенка составит 25%.
Некоторые генетические заболевания встречаются из поколения в поколение и оказывают огромное влияние на семью. Например, гемофилию, называли царской болезнью, потому что она проявлялась у потомков королевы Виктории, одним из них был российский царевич Алексей.
На сегодняшний день мы можем изучить эмбрионы, полученные в рамках ЭКО и выбрать те, которые не несут больных генов или хотя бы несут лишь один больной ген (в этом случае ребенок будет носителем). И переносить в полость матки только здоровый эмбрион
Следующий шаг — это удаление «больного» гена и его замена здоровым. На мой взгляд это то направление, куда будет двигаться медицина – борьба с дефектными генами, предотвращение заболеваний на самом раннем этапе.